Grøn kemi – læren om hvordan kemi udføres bæredygtigt og sikkert – bliver kun vigtigere.
Artiklen har været bragt i Dansk Kemi nr. 4, 2025 og kan læses uden illustrationer, strukturer eller ligninger herunder
(læs originalartiklen her)
Af Christine Brænder Almstrup og Mikael Bols, Kemisk Institut, Københavns Universitet
“Grøn” kemi hentyder ikke til grønne farvede forbindelser, men til en gren af kemien, hvor man kort fortalt forsøger at gøre kemien mere bæredygtig og ufarlig. Hvad “grøn” kemi omfatter, blev defineret i 1990’erne af Paul Anastas og John Warner [1] med de 12 principper vist i figur 1.
Som det fremgår af figuren, har man blandt andet fokus på at mindske mængden af affald fra kemi og anvende mindre farlige kemikalier og opløsningsmidler i kemien. Skønt “grøn” kemi altså ikke er et nyt begreb, er det kun blevet vigtigere og vigtigere siden [2]. Det skyldes, at det er blevet alment accepteret, blandt andet på grund af akkumulationen af drivhusgasser i atmosfæren med klimapåvirkninger til følge, at den nuværende menneskelige aktivitet ikke er bæredygtig.
Kemi spiller sådan en vigtig en rolle i det moderne samfund. Det gælder i høj grad den petrokemiske industri som, udover benzin, olie og gas, leverer de fleste af de organiske kemikalier, vi anvender til fremstilling af tøj, maling, lægemidler og plast. Særligt plast og andre kemisk fremstillede materialer indgår i et utal af produkter lige fra møbler til bærbare computere og mobiltelefoner. Kemi spiller også en rolle i den grønne omstilling. Skal klimaaftrykket af det moderne samfund nedbringes, skal alle disse kemikalier gerne kunne produceres fra noget andet end olie, for eksempel fornybare råvarer som biomasse. Og man bør bruge mindre af dem for derved at forebygge affaldsproduktion.
Fremtidens grønne kemi bør derfor være så effektiv som muligt, så der bruges færrest mulige kemikalier og produceres mindst muligt affald. Et vigtigt begreb i grøn kemi er atomøkonomi, angivet i tabel 1.
Atomøkonomi
En af forudsætningerne for grønne kemiske processer med lav affaldsproduktion er, at de kemiske reaktioner, der udføres, har en god atomøkonomi. Atomøkonomi er en beregning af, hvor mange af atomerne på reaktantsiden der ender i produktet i stedet for som affald eller spildprodukt. Hvis vi ser på reaktionen:
A + B → C + D
hvor A og B er reaktanterne, og C er vores ønskede produkt, så vil atomøkonomi (AØ) beregnes således:
(ligning mangler)
Jo nærmere AØ er på 100 procent, jo bedre siges atomøkonomien at være. Omvendt, jo lavere procenttal atomøkonomi, jo mere affald (stoffet D) danner reaktionen. Atomøkonomien fortæller os, at visse almindelige reaktioner, som for eksempel additionsreaktioner (tabel 1, linje 1), altid vil være grønne, mens substitutionsreaktioner (tabel 1, linje 2) ofte ikke er det. Interessant er det, at vigtige kemiske reaktioner som i sin tid blev belønnet med nobelprisen, ikke nødvendigvis er særligt grønne, men kan være det. For eksempel har Wittig-reaktionen og Grignard-reaktionen (tabel 1), som er nyttige til at etablere nye carbon-carbon bindinger, en forfærdelig atomøkonomi. Til gengæld giver to andre “noble” reaktioner, klikreaktionen og Diels Alder-reaktionen så god en atomøkonomi som muligt, fordi de faktisk er additionsreaktioner.
Fremtidens kemiske processer bør ligne de sidstnævnte reaktioner. Klikreaktionen anvender ydermere katalyse, som også er et vigtigt princip i grøn kemi, fordi det giver mulighed for at forbruge færre kemikalier og derved danne mindre affald.
E-faktor
En anden parameter, der anvendes til at vurdere miljøvenligheden af kemiske processer, er den såkaldte E-faktor (står for environmental factor) [3]. E-faktor er defineret som forholdet mellem massen af det affald, der produceres, og massen af produktet
(ligning mangler)
Det betyder derfor, at jo lavere E-faktor, jo mindre affald producerer den, og jo mere miljøvenlig er processen som udgangspunkt. Dog med det forbehold, at miljøbelastningen af affald kan variere meget. Hvor atomøkonomien betragter kemiske reaktioner eller processer fra et teoretisk synspunkt og således ikke tager højde for effektiviteten/udbyttet eller anvendelsen af opløsningsmidler, så forholder E-faktoren sig til de faktiske forhold og udbytter i reaktionerne. En reaktion med høj atomøkonomi kan have en meget lav E-faktor, men ikke nødvendigvis. Hvis eksempelvis Diels Alder-reaktionen (tabel 1) kan foretages ved blot at blande de to reaktanter i støkiometriske mængder og giver 100 procent udbytte, så vil E-faktoren være nul, hvilket er fremragende. Men hvis man er nødt til at anvende et opløsningsmiddel, som vejer 10 gange så meget som reaktanterne, så bliver E-faktoren pludselig 10 og ikke særlig god.
Plast og affald
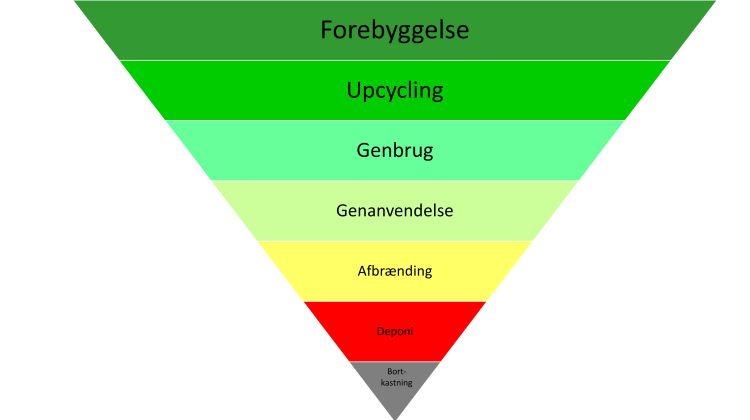
Et af de mest anvendte kemiske produkter er de organiske polymerer, som vi kender som plast. Den årlige produktion af plast er på 300 megaton. Skønt selve produktionen af plast har lav E-faktor og derfor fører til lidt affald, så ender det meste plast efter endt brug som affald. Af alt det plastaffald, der blev produceret i 2023, blev kun 9 procent genbrugt, 19 procent brændt af, 49 procent blev deponeret og 22 procent blev skødesløst bortkastet. Mindre forbrug af plast, og mere genbrug af plast er klart at foretrække. Herefter er genanvendelse at foretrække, mens afbrænding, som genanvender energi, men omdanner plasten til CO2 i atmosfæren, er mindre godt, og deponi eller skødesløs bortkastning er værre (figur 2).
Ved genanvendelse vil man oftest benytte rengjort og sorteret polymer efter en simpel opvarmning og genformning – i praksis vil en sådan genanvendt plast have en lavere kvalitet på grund af urenheder. Alternativt kan man nedbryde polymeren til sine monomere byggesten og så polymerisere den til ny højkvalitetsplast.
Ved upcycling (figur 2) konverteres monomere eller affaldsplasten til mere værdifulde produkter. En oversigt over de hyppigst anvendte plasttyper er samlet i tabel 2.
Da der bruges en bred vifte af plasttyper (tabel 2), er genanvendelse en kompliceret proces, som kræver omhyggelig sortering og rengøring. Bedst er det, hvis plasten kan recycles til monomerer og så repolymeriseres. Men da de fleste plasttyper såsom PE, PP, PS og PVC fremstilles ved fri radikal polymerisering, er depolymerisering yderst vanskeligt. Kun ved polyesteren PET (tabel 2) er depolymeriseringen simpel. Derfor foregår der en rivende forskning i at finde måder at depolymerisere og upcycle plast.
Eksempelvis har John Hartvigs gruppe fra Yale vist, at man ved fiks anvendelse af en iridium-katalysator til at indføre dobbeltbindinger i polymeren og olefin metatese (en reaktion, der omfordeler alkener ved spaltning og gendannelse af carbon-carbon dobbeltbindinger) kan konvertere polyethylen til propen [4]. Da propen er monomeren, der anvendes til fremstilling af polypropylen, en mere værdifuld plast, er der tale om en upcycling af plastaffald. Tilsvarende har Troels Skrydstrups gruppe fra Aarhus Universitet fundet en metode til at depolymerisere epoxy resin til monomeren bisphenol A (figur 3) [5]. Epoxy resin er den plast, som anvendes i vindmøllevinger og som efter endt brug ellers kun kan afskaffes ved deponi.
Plast er et tema, der ofte inddrages i gymnasiets kemiundervisning. Måske kan perspektiverne i grøn kemi også inddrages, hvormed man også inddrager gymnasiets formål, som indbefatter, at eleverne skal ”lære at forholde sig reflekterende og ansvarligt til deres omverden, herunder medmennesker, natur, miljø, klima og samfund, samt til deres udvikling” [6].
Denne artikel er et resume af et læringsforløb for gymnasielærere i kemi, afholdt i regi af STEM Academy Kemi i 2025.
E-mail:
Mikael Bols: bols@chem.ku.dk
Referencer
1. P. Anastas and J. Warner, Green Chemistry: Theory and Practice, Oxford University Press, 1998.
2. Mike Lancaster, Green Chemistry. An introductory text, Royal Society of Chemistry, Cambridge, 3rd edition., 2016.
3. R.A. Sheldon, The E factor at 30: a passion for pollution prevention, Green Chemistry, 2023, 25, 1704-1728.
4. R.J. Conk, S. Hanna, J.X. Shi, J. Yang, N.R. Ciccia, L. Qi, B.J. Bloomer, S. Heuvel, T. Wills, J. Su, A.T. Bell and J.F. Hartwig, Catalytic deconstruction of waste polyethylene with ethylene to form propylene, Science (1979), 2022, 377, 1561-1566.
5. A. Ahrens, A. Bonde, H. Sun, N.K. Wittig, H.C.D. Hammershøj, G.M.F. Batista, A. Sommerfeldt, S. Frølich, H. Birkedal and T. Skrydstrup, Catalytic disconnection of C–O bonds in epoxy resins and composites, Nature, 2023, 617, 730-737.
6. Bekendtgørelse af lov om de gymnasiale uddannelser 2024. https://www.retsinformation.dk/eli/lta/2024/1003.

