Ikke-krystallinske glasmaterialer er typisk noget, vi forbinder med vinduer og skærme, men kan også forbedre ydeevnen af batterier.
Artiklen har været bragt i Dansk Kemi nr. 5, 2025 og kan læses uden illustrationer, strukturer eller ligninger herunder
(læs originalartiklen her)
Af Søren Strandskov Sørensen og Morten Mattrup Smedskjær, Institut for Kemi og Biovidenskab, Aalborg Universitet
I materialeforskningen inden for batterier er der stor interesse i at erstatte den flydende elektrolyt med et fast materiale for at forbedre sikkerheden og energitætheden i nye faststofbatterier [1]. Oftest er fokus på ordnede krystallinske materialer, men ikke-krystallinske glasmaterialer har vist sig at have en række fordele over krystaller [2,3].
Nye batterier kræver nye materialer
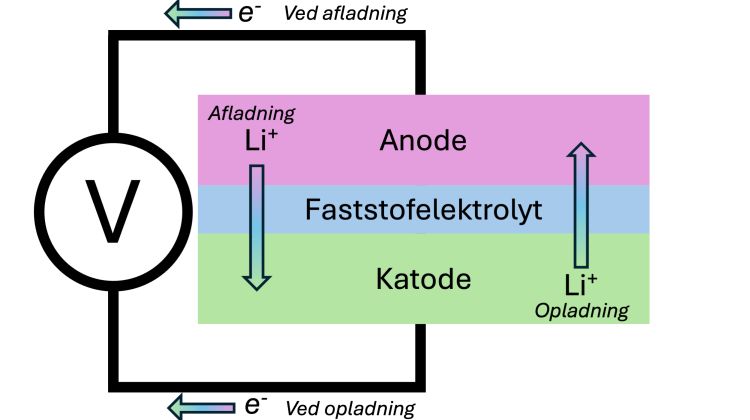
Siden den galvaniske celle lagde grundlaget for den moderne elektrokemi for flere hundrede år siden, er udviklingen af moderne batterier aldrig gået hurtigere. Et af de primære fokusområder er forbedringen af transportable genopladelige batterier, der er blevet en hjørnesten i den grønne omstilling, for eksempel til brug i transportsystemer (biler, tog, osv.). Den oftest anvendte batteriteknologi baserer sig på lithium-ioner, der under afladning bevæger sig fra en faststofanode gennem en elektrolyt, før den inkorporeres i en fast katode. Imens bevæger den tilhørende elektron sig gennem et eksternt kredsløb og afsætter en spænding, der for eksempel kan drive en motor (figur 1).
Selvom Li-ion batteriet har høj energitæthed i forhold til galvaniske celler, er der langt op til energitætheden for eksempelvis flydende brændsler (benzin, diesel, flybrændstof) [4]. En af de store begrænsninger i denne proces er den flydende elektrolyt, der desuden kan udgøre en markant brandfare ved kortslutning. Af denne årsag fokuserer meget materialeforskning på at udvikle en faststofelektrolyt. Denne giver mulighed for at bruge en metalbaseret anode (i stedet for grafit som primært anvendes i dag) og dermed opnå højere energitæthed end det flydende alternativ. Introduktionen af et fast materiale kommer dog med en række nye problemer, blandt andet fordi ionledningsevnen typisk er lavere i faste stoffer sammenlignet med væsker, mens faste stoffer også kan opleve mekaniske brud. For faststofelektrolytter er sidstnævnte et markant problem, der kan nedsætte ydeevnen af batteriet eller ligefrem medvirke til kortslutning.
Fordele ved glas
Historisk har udviklingen af faststofelektrolytter primært fokuseret på krystallinske materialer, hvilket har nogle klare fordele: De kemiske bestanddele og de dannede strukturer kan som oftest løses præcist. Til gengæld er selve ionledningsprocessen relativt kompleks, da større materialevolumener (>>mm3) næsten altid vil bestå af en stor mængde krystaller (polykrystal), hvorfor ionledningsevnen vil være kraftigt afhængigt af morfologi fra nano- til millimeterskala, krystalstørrelser, orientering og graden af ”sammensmeltning” af enkeltkrystaller. Disse problematikker kan ofte overkommes ved brug af glasmaterialer, det vil sige ikke-krystallinske materialer. Disse er produceret ved først at smelte en krystal for derefter at nedkøle væsken så hurtigt, at den ikke når at ordne sig til en krystal. Det dannede faste stof er i den såkaldte glastilstand.
I modsætning til krystaller har glas ikke nogen partikelkornsgrænser, hvilket gør det nemt at forme og danne sammenhængende strukturer af glas. Således kan hele elektrolytten dannes i ét sammenhængende lag med homogene egenskaber. Derudover er glassets egenskaber uafhængige af orientering, hvilket blandt andet viser sig på nanoskala ved, at ioner ikke ledes i velordnede kanaler, som det ellers ofte er tilfældet i krystaller (figur 2).
Computersimuleringer af glaselektrolytter
Der er sket mange fremskridt i forståelsen af ionledning i materialer gennem eksperimentelle analyser, men for at opnå en dybere forståelse af elektrolytmaterialer og forklare eksperimentelle observationer er det ofte nyttigt at benytte sig af såkaldte molekylærdynamiske (MD) simuleringer. MD-simuleringer er i bund og grund simple løsninger af Newtons anden lov (kraft = masse ´ acceleration), hvor man ved hjælp af kraftfelter kan udregne accelerationen for enkelte atomer og herefter fremskrive atompositionerne som funktion af tid. Herefter regnes kræfterne på ny og der itereres fremad.
Problemerne ved MD-simuleringer relaterer sig ofte til rigtigheden af beskrivelsen af kræfterne, men for glas er der en yderligere kompleksitet. Nemlig at man ikke præcist kender materialets atomare struktur, da denne ikke kan ”løses”, ligesom det er almindeligt for krystaller (typisk ved hjælp af røntgendiffraktion). Det betyder, at man er nødt til at simulere en dannelsesprocedure, hvor man typisk smelter et materiale, nedkøler det, og antager, at den indefrosne væskes struktur er en god beskrivelse af glasset – alt sammen inde i computeren.
Om end nøjagtigheden tidligere har været debatteret, har udviklingen af moderne kraftfelter muliggjort MD-simuleringer med tusindvis af atomer i op til flere nanosekunder (1 ns = 10-9 s) med en nøjagtighed tæt på kvantemekaniske beregninger [5]. Det kan lyde som meget kort tid, men det er flere størrelsesordener bedre end for bare få år tilbage. Udviklingen er drevet af øget computerkraft, nye algoritmer, og specielt nye måder at bygge kraftfelter på. Dette muliggør ”lange” simuleringer, hvor man kan studere, hvordan de relevante ioner (typisk Li+ eller Na+) bevæger sig, enten som funktion af temperatur eller under et elektrisk felt, for derved at estimere materialets ioniske ledningsevne – en af de vigtigste parametre for succesfuldt at kunne benytte et materiale som en faststofelektrolyt.
Glas revner stadig
Om end udviklingen af faststofelektrolytter har set massive fremskridt de seneste år, har de stadig problematikker relateret direkte til den faste tilstand. Et typisk problem er, at der kan vokse dendritter af lithium på anoden under opladning. På grund af den relativt lave modstand mod revnevækst (lav brudsejhed) i mange faststofelektrolytter vil disse såkaldte ”dendritter” kunne vokse sig igennem faststofelektrolytten, reducere dens ydeevne og ultimativt kortslutte batteriet ved at forbinde de to elektroder. I vores forskning arbejder vi aktivt på at forstå, hvad der styrer brudsejheden i glasbaserede faststofelektrolytter, hvordan den ændrer sig under battericyklussen, og ultimativt, hvordan den kan forbedres.
Her udnytter vi MD-simuleringer til at estimere brudsejheden ved direkte at ”måle” den kraft, der skal til, for at en revne gror i en given faststofelektrolyt. Et eksempel på en sådan simulering ses i figur 3, hvor simuleringsboksen med en indsat revne (hulrum i strukturen) løbende strækkes, hvorfor revnen vokser og til sidst kløver elektrolytten. MD-simuleringerne gør det muligt at teste et stort antal systemer på relativt kort tid sammenlignet med eksperimenter. Dette har blandt andet gjort det muligt at påvise, hvordan brudsejheden falder, når ionledningsevnen stiger i et ionledende glas baseret på Li2S-SiS2 [6]. Vi har udnyttet det samme princip til at studere andre systemer med relevans som faststofelektrolytter, blandt andet glaskeramiske materialer (dvs. delvist amorfe, delvist krystallinske) baseret på lithium aluminotitanofosfat, hvor glas-krystal grænsefladen giver en unik høj brudstyrke. Ved hjælp af simuleringerne har vi tilskrevet denne effekt til en forøget mulighed for flere af kationerne (Al, Ti) til skifte koordinationstal under deformeringen og derved fordele energien i grænsefladerne mellem glas og krystal [7,8].
Opsamling
Glasmaterialer har vist sig interessante som materialer i moderne faststofbatterier. Deres uordnede struktur giver unikke muligheder for at finjustere deres egenskaber, men besværliggør deres design alene baseret på eksperimentelle studier. I vores forskning har vi fokus på at forstå brudmekanismerne af forskellige faststofelektrolytter, blandt andet ved hjælp af computersimuleringer på nanoskala. Her kan vi følge, hvordan de atomare bindinger brydes, når en revne vokser og derved analysere, hvilke strukturelle dele af en elektrolyt der er med til at forbedre modstanden mod revnedannelse, mens ionledningsevnen og ydeevnen af batteriet stadig opretholdes.
E-mail:
Søren Strandskov Sørensen: soe@bio.aau.dk
Morten Mattrup Smedskjær: mos@bio.aau.dk
Referencer
1. Kalnaus S, Dudney NJ, Westover AS, Herbert E, Hackney S (2023) Solid-state batteries: The critical role of mechanics. Science, 381: eabg5998.
2. Wang Z, Luo S-hua, Zhang X, Guo S, Li P, Yan S (2023) Glass and glass ceramic electrodes and solid electrolyte materials for lithium ion batteries: A review. Journal of Non-Crystalline Solids, 619, 122581.
3. Zhao Q, Stalin S, Zhao CZ, Archer LA (2020) Designing solid-state electrolytes for safe, energy-dense batteries. Nature Reviews Materials, 5(3):229-252.
4. Janek J, Zeier WG (2016) A solid future for battery development. Nature Energy, 1(9):16141.
5. Unke OT, Chmiela S, Sauceda HE, Gastegger M, Poltavsky I, Schütt KT, Tkatchenko A, Müller KR (2021) Machine Learning Force Fields. Chemical Reviews, 121(16):10142-.
6. Sørensen SS, Boysen D, Lindbjerg ER, Mortensen HN, Lippert KT, Diget SM, Konieczna Z, Micoulaut M, Smedskjaer MM (2025) Balancing fracture toughness and ionic conductivity in lithium thiosilicate glassy electrolytes. Physical Chemistry Chemical Physics, 27: 10331-10341.
7. Chen Z, Du T, Krishnan NMA, Smedskjaer MM (2023) Enhanced bond switching at complexion layer facilitates high fracture energy of LATP solid-state electrolytes. Journal of Materials Chemistry A, 12(5):3061-3071. 8. Famprikis T, Canepa P, Dawson JA, Islam MS, Masquelier C (2019) Fundamentals of inorganic solid-state electrolytes for batteries. Nature Materials, 18(12):1278-1291.

